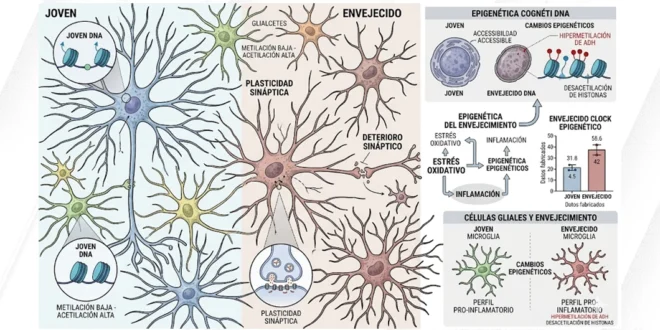
El envejecimiento cerebral dejará de ser un enigma gracias al primer atlas epigenético unicelular. Un equipo internacional coordinado por el Instituto Salk ha logrado mapear con precisión quirúrgica cómo el paso del tiempo altera la estructura del ADN en el cerebro, abriendo la puerta a diagnósticos tempranos de enfermedades como el Alzheimer y la esclerosis lateral amiotrófica.
El envejecimiento afecta al ADN cerebral principalmente a través de la pérdida de metilación, un proceso químico que funciona como un candado de seguridad. Al debilitarse estos sellos con la edad, fragmentos genéticos que deberían permanecer silenciados se activan, provocando inestabilidad genómica e inflamación crónica en las células nerviosas.
Los genes saltarines y el caos celular
Uno de los hallazgos más relevantes de este atlas es la reactivación de los elementos transponibles, conocidos coloquialmente como «genes saltarines». Estos segmentos ocupan casi la mitad del genoma humano y, en un cerebro joven, están reprimidos por etiquetas químicas.
Con el paso de las décadas, la pérdida de metilación permite que estos genes se muevan o se expresen, alterando el equilibrio celular. Esta desregulación no ocurre de forma uniforme; el estudio identifica «puntos calientes» de deterioro que varían según la región anatómica y el tipo de célula, lo que explica por qué ciertas funciones cognitivas fallan antes que otras.
La glía: el eslabón más vulnerable
Contrario a lo que se pensaba, las neuronas no son las únicas protagonistas del deterioro. El atlas revela que las células no neuronales, específicamente la glía, muestran ritmos de envejecimiento mucho más acelerados. La glía es responsable de proteger y alimentar a las neuronas, además de regular la respuesta inmunitaria.
Los investigadores observaron que las células gliales en la parte posterior del cerebro presentan niveles de inflamación y desregulación genética significativamente mayores que las situadas en el área frontal. Esta vulnerabilidad diferencial sugiere que el entorno celular, o el «terreno» donde habitan las células, determina la velocidad del declive cognitivo.
Arquitectura genómica como biomarcador
El estudio también introduce un concepto técnico crucial: los dominios de asociación topológica (TAD). Imagine que el ADN es un edificio con paredes internas que organizan el espacio. El fortalecimiento de los límites de estos dominios actúa como un biomarcador de alta precisión para medir la edad biológica del cerebro.
Al cambiar la arquitectura tridimensional del genoma, las conexiones y la comunicación interna de la célula se ven comprometidas. Identificar estos cambios estructurales permite a los científicos visualizar el deterioro antes de que los síntomas clínicos sean evidentes en el paciente.
Preguntas Frecuentes sobre ADN y envejecimiento cerebral
¿Cómo ayuda este atlas a curar el Alzheimer?
El atlas permite identificar las etiquetas químicas específicas que fallan al inicio de la enfermedad. Esto facilita el diseño de terapias que busquen «reiniciar» el epigenoma, restaurando los candados químicos del ADN antes de que el daño sea irreversible.
¿Es el envejecimiento cerebral igual en todas las personas?
No. Aunque el atlas se realizó en modelos animales, demuestra que incluso dentro de un mismo cerebro, el envejecimiento es heterogéneo. Factores como la ubicación celular y el tipo de célula (neurona vs. glía) definen la velocidad del deterioro.
¿Qué son los cambios epigenéticos en el ADN?
Son modificaciones químicas que no alteran la secuencia de la información genética, pero sí determinan si un gen se activa o se apaga. Es la diferencia entre tener las instrucciones de un mueble y decidir qué piezas armar en cada momento.
 IMPACTO PANAMÁ
IMPACTO PANAMÁ